|
Zaman Yolculuğunu Araştırma Merkezi © 2005 Cetin BAL - GSM:+90 05366063183 -Turkey/Denizli |
Atom Modelleri
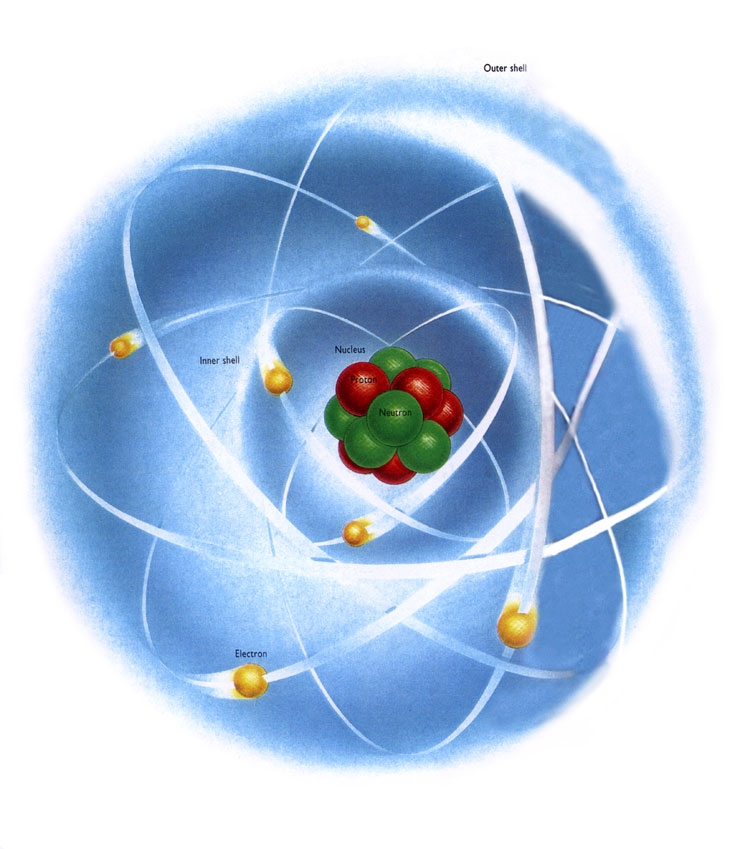
Rutherford Atom Modeli: Çekirdekli Atom Modeli.
Rutherford'un öğrencileri Geiger ve Marsden, alfa kaynağını, üzerinde küçük
bir delik bulunan kurşun perdenin arkasına yerleştirdiler. Böylelikle hedefi
küçültmek ve ince bir alfa parçacıkları demeti elde etmek amaçlanmıştı.
Altın yaprağın öbür yanına, kendisine alfa parçacığı çarptığı zaman görünür
ışık parıltısı veren, hareketli, çinko sülfürlü ekran yerleştirilmişti.
Beklenen şey, alfa parçacıklarının çoğunun yaprak içinden doğrudan geçeceği,
belki bazılarının çok küçük sapmalara uğrayacağıydı. Bu beklenti, Thomson
Atom Modeli'nin sonucudur. Çünkü Thomson Atom Modeli doğruysa, ince metal
levhadan geçen alfa parçacıkları üzerine yalnızca zayıf elektriksel
kuvvetler etkir ve alfa parçacıklarının momentumları, bunların ilk
yollarından çok küçük sapmalar olacak şekilde ilerlemelerini sağlar.
Geiger ve Marsden, alfa parçacıklarının çoğunun sapmadan ilerlediğini,
bazılarının çok geniş açılarda saçıldığını, hatta çok az bir kısmının
gerisin geriye döndüğünü gördüler. Geliş doğrultusuyla 180 derece açı
yapacak şekilde geri saçılan bu parçacıklar, direkt olarak bir çekirdeğe
yönelir ve kafa kafaya çarpışma olur.
Bu modelde, pozitif yüklü alfa parçacıklarıyla atomdaki elektronların
ilişkisi merak edilir. Elektronlar pek küçük kütleli olduğu için alfa
parçacıklarının hareketinde önemli bir etkide bulunmaz.
Alfa parçacıkları, elektronlardan 7.000 defa daha ağır kütleli
parçacıklardı. Üstelik bu deneyde kullanılan alfa parçacıklarının hızı
yüksekti. Alfa parçacıklarını bu derece saptırabilmek için büyük kuvvetler
uygulanması gerektiği açıktı. Bu kuvvetlerin Thomson Atom Modeli'ndeki
elektriksel kuvvetlere göre 100 milyon kat güçlü olduğu hesaplanıyordu.
Rutherford, sonuçları açıklamak için, bir atomun pozitif yüklü bir çekirdek
ile biraz uzaktaki elektronlardan oluştuğunu önerdi. Buna göre atomun
pozitif yükü ve kütlesi atom çekirdeğinde toplanmıştı.
Geiger ve Marsden'in deneyleri, daha sonraki benzer çalışmalar, hedefleri
oluşturan değişik metallerin çekirdekleri hakkında bilgiler verdi. Bir alfa
parçacığının, bir çekirdek yakınından geçerken uğradığı sapma (karşılaştığı
elektriksel alan), çekirdek yükünün büyüklüğüne bağlıdır. Bu sapmalardan
yanrarlanılarak çekirdek yükü ve çekirdek boyutu konusunda bilgiler elde
edildi.
Çekirdek kuvvetleri çok kısa mesafeli kuvvetlerdi. Atom çekirdeğiyle ilgili
kilometre taşı sayılan diğer olaylar şunlardır:
1930 yılında Cockroft ve Walton hızlandırılmış parçacıkların kullanılmasıyla
gerçekleştirlen çekirdek tepkimelerinin gözlenmesi
1932 yılında Chadwick'in nötronu bulması
1933 yılında Joliot ve İrene Curie'nin yapay radyoaktifliği bulması
1938'de Hahn ve Strassman'ın çekirdek bölünmesini (çekirdek fisyonunu)
bulması
1942 yılında Fermi ve ekibinin kontrol edilebilen ilk fisyon reaktörünün
geliştirilmesi
Rutherford’un saçılma deneyleri ilgi çekici idiyse de, klasik fizik
açısından onun gezegensel resmi sanıldığı kadar dengeli değildi. Doyurucu
olmayan durum kısa sürede değişti. 1912 cıvarında Rutherford, Manchester’dan
arkadaşı Boltwood’a şöyle yazıyordu: "Bir Danimarkalı olan Bohr,
Cambridge’den çıkmış, radyoaktif çalışmada bazı deneyler yapmak üzere buraya
geliyor".
Cambridge’de, J.J. Thomson’un bir öğrenci olan Niels Bohr, kendi
memleketine, Kopenhag’a dönmeden önce, Manchester’da yarım yıldan az bir
süre kaldı. Ancak, kısa ziyaretine rağmen, Rutherford genç Danimarkalı
üzerinde etkili oldu.
Bohr'un ilgisini çekmiş olan atomik yapı problemi, yaratıcı cesaretli bir
adım attı: Klasik fiziğin bazı kurallarını bıraktı ve onun yerine atomik
yapı problemine Planck’ın ve Einstein’in Kuantum Kuramı'nı uyguladı. Dikkate
değerdir ki o zamanlar bilinen Kuantum Kuramı'nın birkaç özelliği problemi
çözebilirdi (Klasik fizikle çelişki konusuna aldırış edilmediği sürece).
Bohr, basitçe, çekirdek etrafındaki yörüngelerdeki elektronların ışık
yaymadıklarını ve atomların yaydığı ışığın bir başka fiziksel yapının sonucu
olduğunu varsaydı. Bohr, Planck’ın enerjinin kuantlaşması fikrinin,
elekronlar için ancak belli yörüngelerin mümkün olduğu anlamına geldiğini
gösterdi. Atomların kararlılığını korumak için Bohr, yörüngedeki elektronun
onun altına düşemeyeceği en düşük enerjili yörünge konusunda bir önermede
bulundu.
Bir elektron daha yüksek bir yörüngeden, daha alçağına düşerken, böylece
enerji kaybederken, bu elektronu taşıyan atom ışık yayar, bu da kaybedilen
enerjiyi taşır. Yalnızca belli elektron yörüngelerine izin verildiği için,
elektronların yörüngeler arasında yalnız belli sıçramalar olabilir ve sonuç
olarak, yayılan ışığın enerjisi kuantlaşır (Nicelik olarak ifade
edilebilir).
Işığın enerjisi, rengi ile bağlantılı olduğu için, atomlar tarafından ancak
belli renklerde ışık yayılabilir. Bu şekilde Bohr’un teorik Atom Modeli,
gizemli tayf çizgilerinin varlığını açıklamaktadır. Her farklı atomun tek ve
belli renklerde ışık yaydığını ifade eden deneysel olarak gözlemlenmiş
gerçek, atomların kuantum yapısını açığa çıkarmıştır.
Bohr’un atomunun enerji düzeylerini imgelemenin bir yolu, harp gibi, yaylı
bir müzik enstürmanı düşünmektir. Çalındığı zaman her yaydan belli bir
titreşim veya ses çıkar. Benzer şekilde bir elektron, atomdaki yörüngelerde
atlarken, belli bir titreşimi veya rengi olan ışık yayılması olur. Bu da
kesintili ışık tayfının kaynağıdır.
Bohr yeni fikirlerini, tek bir protonla onun çevresinde yörüngede tek bir
elektronu olan en basit atoma, hidrojene uyguladı. Böyle basit bir atom
incelemenin avantajı, elektronun izin verilen yörüngelerinin kesin olarak
hesaplanabilir olması ve bu nedenle de hidrojenden çıkan ışık tayfının
belirlenebilmesidir.
Bohr’un kendi teorik Atom Modeli'ne dayanan hidrojen ışık tayfı ile ilgili
hesapları, deneysel olarak gözlemlenmiş olan tayfa yeterince uygun sonuç
verdi. Teori ile deney arasında böyle uyum rasgele olamazdı. Bu durum,
Bohr’un, Kuantum Teorisi'nden aldığı fikirler bileşiminin doğru çıktığı
anlamına geliyordu.
Kuramsal fizikçiler, Bohr’un fikirlerini aldılar ve daha karmaşık atomlara
uyguladılar. Ancak, her büyük bilimsel ilerleme gibi, Bohr’un modeli pek çok
yeni soruya (Daha önce sorulamayan sorulara) yol açtı. Bir elektron ne zaman
yörüngesini değiştirip atomdan ışık yayılmasına yol açar? Yayılan ışık hangi
doğrultuda ilerler ve neden?
Bu sorular Einstein’ı zorladı. Klasik fiziğe göre, hareketin yasaları atom
gibi bir fiziksel sistemin gelecekteki davranışını kesin olarak belirler.
Fakat ışık yayan atomlar ani ve önceden belirlenmemiş şekilde hareket ediyor
görünüyorlardı. Atomlar sıçrıyor. Fakat neden ve hangi yönde? Einstein, aynı
aniliğin radyoaktivitenin de özelliği olduğunu kavradı.
Başlangıçta fizikçiler, atomların davranışını klasık elektromanyetizm
teorisi çerçevesine uydurmaya çalıştılar ve ışık kuantası kullanmadan,
kuantum sıçramaları bilmecesini yanıtlamak için umutsuz girişimlerde
bulundular. 1924'te Niels Bohr, Hendrik Kramers ve John Slater, atom
düzeyinde enerji ve momentumun korunumu yasalarını terketme pahasına bu
yaklaşımı savunan bir yazı yazdılar.
Bu devrimci bir öneriydi. Çünkü bu yasalar en iyi test edilmiş fizik yasalar
aasında bunuyorlardı. Bu önerini yapıldığı zamanda, korunum (sakınım)
yasalarını tek tek atomik süreçler için geçerli olduğunu gösteren hiçbir
doğrudan deneysel kanı olmamıştı. Ancak bu kısa sürede gerçekleşti.
Arthur H. Compton ve A. W. Simon, elektronlardan tek tek fotonlar, ışık
parçacıkları saçılmasını sağladılar. Tek tek elektronların izlerini
görüntüleyen bir cihaz olan Wilson Bulut Bölmesi kullanarak, yüksek
hassaslık derecesi ile tek tek atomik süreçler için korunum yasalarını
doğruladılar. Fizikçilerin çoğu için 1925'te yapılan bu deneyler,
Einstein’ın 1905 yılındaki ışık kuantumu önerisini destekledi.
Rutherford ve Compton’ununkiler gibi çok sayıda yeni atomik deneyle, atomun
yapısı açağa çıkarılmıştı. Bu deneyler, teorik fizikçileri yeni ve
bilinmeyen bir dünyaya geçmeye zorladı; alışılmış olar klasik fiziğin
yasaları artık işlemiyor görünüyordu. Atomda insan zihni yeni bir mesajı
almıştı. Atomik mikrodünyanın yapısında yeni bir fizik açığa çıktı.
Yüzyıllarca deney ve fiziksel teorilerle desteklenen determinizmin dünya
görüşü yıkılmak üzereydi.
Bohr, Compton ve Simon’un deneylerinin sonuçlarının, hem Korunum Yasalarının
doğruluğu, hem des Işık Kuantumu veya fotonun varlığı anlamına geldiğini
kabul etti. Temmuz 1925'te şu sonucu özetledi: "Klasik elektrodinamik
teorinin gerekli genelleşmesinin, doğanın tanımını bu güne kadar üzerine
kurulmuş olduğu kavramlarda köklü bir devrimi gerektirdiği gerçeğine hazır
olunmalıdır." Bohr bu devrime hazırdı. Bu, kısa sürede gerçekleşti. Bunun
ilk adımı halihazırda, kuzey denizinde bir küçük adada atılmıştı."
Saçıcı metal yapraktan, floresans ekrana gelen alfa parçacıklarının, birim
yüzeye düşen sayısı, metal yaprağın kalınlığıyla, metal yaprakta birim
hacimdeki atom sayısıyla ve atomdaki çekirdek yükünün karesiyle doğru
orantılıdır. Deneyler pek çok çekirdeğin yaklaşık küresel geometriye sahip
oldukları ve tüm çekirdeklerin yaklaşık aynı yoğunluğa sahip olduğunu
gösterdi.
Thomson, kendi atom modelinde, elektronların pozitif madde içinde gömülü ve
bu nedenle de hareket edemez olduğunu tasarlamıştı. Rutherford Modeli'nde
elektronlar durgun olamaz. Elektronlar, elektrostatik çekim sonucu spiral
bir hareketle çekirdeğe düşecektir (klasik fizik yasalarına göre). Oysa
atomla,r yadsınamaz kararlılıklarıyla ortadadır.
Rutherford modeli şu iki soruyu yanıtlayamıyordu:
Elektronlar, çekirdek üzerine düşmeden nasıl hareket ediyor?
Çekirdek boyutu, on üzeri eksi ondört metre ve daha küçük boyutlarda olduğu
halde pozitif yük, bu küçük ve yoğun hacimde nasıl dağılmadan durabiliyordu?
Başka bir kaynaktan:
1911 Rutherford'un öğrencileri Geiger ve Marsden, alfa kaynağını, üzerinde küçük bir delik bulunan kurşun perdenin arkasına yerleştirdiler. Böylelikle hedefi küçültmek ve ince bir alfa parçacıkları demeti elde etmek amaçlanmıştı. Altın yaprağın öbür yanına,kendisine alfa parçacığı çarptığı zaman görünür ışık parıltısı veren, hareketli, çinko sülfürlü ekran yerleştirilmişti. Beklenen şey, alfa parçacıklarının çoğunun yaprak içinden doğrudan geçeceği, belki bazılarının çok küçük sapmalara uğrayacağıydı. Bu beklenti Thomson atom modelinin sonucudur. Çünkü Thomson atom modeli doğruysa, ince metal levhadan geçen alfa parçacıkları üzerine yalnızca zayıf elektriksel kuvvetler etkir ve alfa paçacıklarının momentumları, bunların ilk yollarından çok küçük sapmalar olacak şekilde ilerlemelerini sağlar. Geiger ve Marsden, alfa parçacıklarının çoğunun sapmadan ilerlediğini, bazılarının çok geniş açılarda saçıldığını, hatta çok az bir kısmının gerisin geriye döndüğünü gördüler. Geliş doğrultusuyla 180 derece açı yapacak şekilde geri saçılan bu parçacıklar, direkt olarak bir çekirdeğe yönelir ve kafa kafaya çarpışma olur. Bu modelde pozitif yüklü alfa parçacıklarıyla atomdaki elektronların ilişkisi merak edilir. Elektronlar pek küçük kütleli olduğu için alfa parçacıklarının hareketinde önemli bir etkide bulunmaz. Alfa parçacıkları, elektronlardan 7.000 defa daha ağır kütleli parçacıklardı. Üstelik bu deneyde kullanılan alfa parçacıklarının hız yüksekti. Alfa parçacıklarını bu derece saptırabilmek için büyük kuvvetler uygulanması gerektiği açıktı. Bu kuvvetlerin Thomson atom modelindeki elektriksel kuvvetlere göre 100 milyon kat güçlü olduğu hesaplanıyordu! Rutherford, sonuçları açıklamak için, bir atomun pozitif yüklü bir çekirdek ile biraz uzaktaki elektronlardan oluştuğunu önerdi. Buna göre atomun pozitif yükü ve kütlesi atom çekirdeğinde toplanmıştı. .Geiger ve Marsden'in deneyleri, daha sonraki benzer çalışmalar, hedefleri oluşturan değişik metallerin çekirdekleri hakkında bilgiler verdi. Bir alfa parçacığının, bir çekirdek yakınından geçerken uğradığı sapma(karşılaştığı elektriksel alan), çekirdek yükünün büyüklüğüne bağlıdır. Bu sapmalardan yararlanılarak çekirdek yükü ve çekirdek boyutu konusunda bilgiler elde edildi. Çekirdek kuvvetleri çok kısa mesafeli kuvvetlerdi.
Atom çekirdeğiyle ilgili kilometre taşı sayılan diğer olaylar şunlardır:
1. 1930 yılında Cockroft ve Walton hızlandırılmış parçacıkların kullanılmasıyla gerçekleştirilen çekirdek tepkimelerinin gözlenmesi
2. 1932 yılında Chadwick'in nötronu bulması
3. 1933 yılında,Joliot ve İrene Curie'nin yapay radyoaktifliği bulması
4. 1938'de Hahn ve Strassman'ın çekirdek bölünmesini (çekirdek fisyonunu) bulması
5. 1942 yılında Fermi ve ekibinin kontrol edilebilen ilk fisyon reaktörünün geliştirilmesi
“Rutherford’un saçılma deneyleri ilgi çekici idiyse de klasik fizik açısından onun gezegensel resmi sanıldığı kadar dengeli değildi. Doyurucu olmayan durum kısa sürede değişti. 1912 cıvarında Rutherford, Manchester’den arkadaşı Boltwood’a şöyle yazıyordu: “Bir Danimarkalı olan Bohr,Cambridge’den çıkmış, radyoaktiflik konusunda bazı deneyler yapmak üzere buraya geliyor”. Cambridge’de J.J. Thomson’un öğrencisi olan Niels Bohr, kendi memleketine, Kopenhag’a dönmeden önce, Manchester’da yarım yıldan az bir süre kaldı. Ancak, kısa ziyaretine rağmen, Rutherford genç Danimarka’lı üzerinde etkili oldu.Çok geçmeden 1913 yılında Bohr,kendi adıyla anılan atom kuramını ortaya attı.
Hiçbir yazı/ resim izinsiz olarak kullanılamaz!! Telif hakları uyarınca bu bir suçtur..! Tüm hakları Çetin BAL' a aittir. Kaynak gösterilmek şartıyla siteden alıntı yapılabilir.
The Time Machine Project © 2005 Cetin BAL - GSM:+90 05366063183 -Turkiye/Denizli
Ana Sayfa /
index /Roket bilimi /![]() E-Mail /CetinBAL/Quantum Teleportation-2
E-Mail /CetinBAL/Quantum Teleportation-2
Time Travel Technology /Ziyaretçi Defteri /UFO Technology/Duyuru